morfoloji
Makroskobik seviyede, Alzheimer hastalığında, frontal, temporal ve pariyetal loblarda daha belirgin olan parietal olukların genişlemesiyle karakterize, değişken derecelerde atrofi (doku veya organların kütlesinin azalması) kortikal gözlemleyebiliriz. Bu atrofi, parankim kaybına ikincil ventriküler boşlukların genişlemesiyle telafi edilir (Şekil 1). Özellikle, hastalığın ileri evrelerinde, hastalığın erken evrelerinde başlayan müdahaleleri göz önüne alındığında, hipokampus, entorinal korteks ve amigdala dahil olmak üzere medial temporal lobun yapıları ciddi atrofidir.
Ayrıca, Alzheimer hastalığı ayrıca, hücre dışı senil plaklar ve histolojik tanı için temeli temsil eden hücre içi nörofibriler kümeleri olarak bilinen mikroskobik değişiklikler de sunar. Daha sonra, hastalığın ilerlemesiyle birlikte, aynı bölgelerde, gliosis ile birlikte ciddi bir nöronal kayıp, nöroliz hücrelerinin, yani sinir dokusunun destekleyici stroma'sını oluşturan hücrelerin, yani reaktif bir doğada dolaşımda veya yaygın çoğalmanın, nörofibriler plak ve kümelerin varlığı daha fazladır.
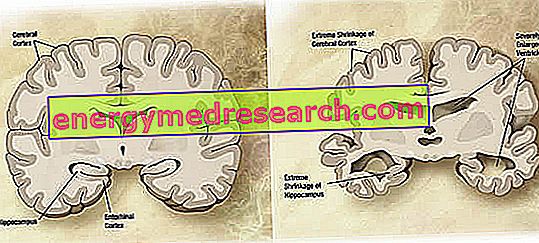
Şekil 1. Beynin koronal kesiti: AD'den etkilenen normal beyin ile beyin arasındaki farklar (görüntü kaynağı wikipedia).
Patogenez
Alzheimer hastalığı esas olarak iki tipik lezyonla karakterize edilir: hiperfosforile edilmiş tau proteininin oluşturduğu intranüronal nörofibriler kümelerinden oluşan esasen amy-amiloid peptidi (Aβ) ve intranöronal nörofibriler kümelerinden oluşan hücre dışı birikimi
- Senil plakları, hipokampus, amigdala ve neokortek gibi serebral alanların seviyesinde bulunabilir.
Ap peptidi, amiloid protein prekürsörünün (APP) proteolitik bir kesiminden, β-sekretazdan türetilir. Bu kesim, daha sonra farklı uzunluktaki Aβ parçalarını üretmek için sec-sekretaz ile kesilmiş olan 99 artıktan (CTF veya C99) bir terminal karboksi fragmanı oluşturur. En bol miktarda bulunan Aβ türünün Aβ40 fragmanından oluştuğu bilinmektedir. Proteolitik kesmeden oluşan ve A40'tan daha az olmayan bilinen bir diğer fragman, Alzheimer hastalığı olan bir bireyin beyninde Aβ türü olarak biriken amiloid fibrillerinin oluşumuna daha eğilimli olan Ap42'dir.
- Alzheimer hastalığında mevcut olan bir diğer bileşen, nöronların sitoplazmasında bulunan filament demetlerinden oluşan nörofibriler kümelerdir. Nörofibriler kümeler çözünmez ve in vivo proteoliz işlemlerine karşı dirençli görünmektedir, böylece nöronal ölümden sonra uzun süre doku bölümlerinde mevcut kalmaktadır. Yapı gözlemlendiğinde, fibril kütleleri, çift sarmallı filamentlerden ve benzer bileşimin lineer filamanlarından oluşur. Kompozisyonu analiz ederek, çift sarmallı filamentler daha fazla hiperfosforile edilmiş tau proteinden oluşur. Tau, montajını kolaylaştıran mikrotübüller ile ilişkili olan bir aksonal proteindir.
Alzheimer hastalığında diğer önemli nöropatolojik değişiklikler mitokondriyal fonksiyon bozukluğu, oksidatif nöronal hasar, sinaptik kayıp ve aksonal dejenerasyondur.
Nörokimyasal yönleri
Daha önce açıklandığı gibi, APP öncülünün proteolitik kesmesinden türetilen AP peptidi, Alzheimer hastalığının nörotoksik bir bileşenini temsil eder . Spesifik olarak, Aβ'nin normal beyin fonksiyonları için önemli olabileceği ve bazı konsantrasyonları aşması halinde nörotoksik hale gelebileceği varsayılmıştır. Ek olarak, hem agregalar hem de farklı Ap izoformları, hastalığın sonraki aşamalarında belirleyen ve katılan farklı bir biyolojik, fizyolojik veya patolojik role sahip olabilir. Aslında, Ap'nin bir nöromodülatör görevi gördüğü, bazı nörotransmiterlerin belirgin nörotoksisite belirtileri yokluğunda salınımını etkilediği gözlenmiştir.
Örneğin, Aβ'nin nöromodülatör rolü, fizyolojik bağlamda, nörotransmitter sisteminin doğru dengesi için önemli bir öneme sahip olabilir. Aslında, bu sistemin nörotransmiterler, sinir sistemini oluşturan hücreler, nöronlar arasında sinaptik iletim yoluyla bilgi ileten maddelerden oluştuğu bilinmektedir.
Patolojik koşullarda, bunun yerine, AP aracılı sinaptik geçiş, nörodejeneratif olaylardan önce nörotransmisyonun değiştirilmesiyle ilişkili olabilir. Bu değişikliklerin bir sonucu olarak, etkilenen nörotransmitter sistemlerine ve ilgili farklı beyin alanlarına bağlı olarak erken bilişsel ve bilişsel olmayan bozukluklar ortaya çıkabilir.
Nörotransmitter sistemlerinin ve Alzheimer hastalığından etkilenen bireylerin beyinlerinde sinyal iletim mekanizmasındaki değişiklikler çok karmaşıktır. Değiştirilen sistemlerden biri, nörotransmiter asetilkolinini içeren kolinerjik sinyalizasyon sistemini dikkate almaktadır. Aslında, Alzheimer hastalığından etkilenen bireylerin korteks ve hipokampus düzeyinde kolinerjik geçişinin azaldığı, öğrenme ve hafıza gibi olaylardan sorumlu beyin alanlarının azaldığı gösterilmiştir. Bu nörotransmitter sistemine ek olarak, Alzheimer hastalığında noradrenerjik serotoninerjik sistemin yanı sıra glutamat ve GABA seviyesinde de değişiklikler gözlenmiştir.